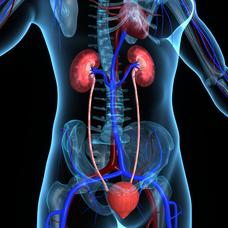
Spätfolgen an den Nieren
Autor: Christine Vetter, Maria Yiallouros, Redaktion: Maria Yiallouros, Freigabe: Prof. Dr. med. Thorsten Langer, Zuletzt geändert: 25.09.2017 https://kinderkrebsinfo.de/doi/e131789
Inhaltsverzeichnis
Einleitung
Der Mensch besitzt im Normalfall zwei Nieren. Sie liegen links und rechts der Wirbelsäule im hinteren Bauchraum. Zu den Hauptaufgaben der Nieren gehört es, das Blut zu filtern. Sie kontrollieren dabei zum einen den Wasser- und Mineralstoffhaushalt des Körpers, zum anderen bringen sie Abfallprodukte des Stoffwechsels mit dem Urin (Harn) zur Ausscheidung.
Um diese Aufgaben erfüllen zu können, besitzt jede Niere etwa eine Million Nephrone. Jedes Nephron besteht aus einem Filterelement, dem so genannten Nierenkörperchen (Glomerulum), und einem sich daran anschließenden Kanalsystem, dem Nierenkanälchen (Tubulus).
Im Bereich des Nierenkörperchens, das aus einem Knäuel feiner Blutgefäße (Kapillaren) besteht, wird kontinuierlich der so genannte Primärharn aus dem Blut gefiltert. Er besteht vor allem aus Wasser und darin gelösten kleinen Molekülen (zum Beispiel Elektrolyten, Aminosäuren, Glukose, Harnstoff) und entspricht damit in seiner Zusammensetzung ungefähr dem Blutplasma. Große Moleküle (wie Blutkörperchen und Proteine) können den Filter nicht passieren.
Auf dem Weg durch die Nierenkanälchen werden bestimmte, für den Körper wertvolle Stoffe aus diesem Primärharn wieder in den Blutkreislauf zurückgeholt, darunter Nährstoffe (wie Aminosäuren, Glukose, Elektrolyte) und der größte Teil (99 %) des Wassers und der Salze. Gleichzeitig werden nicht mehr benötigte oder giftige Substanzen (Stoffwechselendprodukte wie Harnsäure, Medikamente) direkt vom Blut ins Filtrat abgegeben. Auf diese Weise entsteht der eigentliche Harn (auch Sekundär- oder Endharn genannt). Er sammelt sich im Nierenbecken und wird über den Harnleiter zur Harnblase geleitet.
Die Nieren bilden bei Erwachsenen täglich etwa 180 Liter Primärharn. Nur etwa ein Prozent davon (1,5 Liter) gelangt als Sekundärharn in die Harnblase und wird als Urin ausgeschieden.
Gut zu wissen: Die Nieren haben – neben ihrer Ausscheidungsfunktion und ihrer Rolle bei der Aufrechterhaltung des Wasser- und Salzhaushalts – vielfältige weitere Aufgaben. Sie bilden zum Beispiel Hormone, die dafür sorgen, dass der Blutdruck reguliert wird und dass rote Blutzellen im Knochenmark gebildet werden. Auch am Knochenstoffwechsel sind die Nieren (durch die Aktivierung von Vitamin D) beteiligt.
Mögliche Ursachen von Spätfolgen
Sowohl eine Chemotherapie mit bestimmten Medikamenten als auch eine Strahlentherapie im Nierenbereich können die Niere schädigen. Wenn beide Therapieformen in Kombination eingesetzt werden, erhöht sich das Risiko einer Nierenschädigung.
Chemotherapie
Bestimmte Medikamente, die bei der Chemotherapie eingesetzt werden, können sowohl die kleinen Nierenkörperchen als auch die Nierenkanälchen schädigen. Das Filtersystem der Niere kann dadurch so gestört sein, dass Stoffe, die eigentlich im Körper noch gebraucht werden, mit dem Urin ausgeschieden werden, während andererseits Substanzen, die zur Ausscheidung gelangen sollten (wie Abfallprodukte und Giftstoffe), im Körper bleiben und dort Schaden anrichten (siehe auch Abschnitt "Krankheitsbilder")
Zu den wichtigsten nierenschädigenden Zytostatika zählen platinhaltige Medikamente (Cisplatin, Carboplatin) und Ifosfamid.
Platinderivate wirken sich vor allem auf die Nierenkörperchen (Glomeruli) aus und beeinträchtigen so die Bildung des Primärharns. Cisplatin ist dabei insgesamt toxischer als Carboplatin. Daher versucht man, Cisplatin zunehmend durch Carboplatin zu ersetzen, wenn dadurch der Therapieerfolg nicht beeinträchtigt wird. Ifosfamid schädigt dagegen die Zellen der Nierenkanälchen (Tubuli), wodurch diese ihre Aufgaben bei der Rückgewinnung wichtiger Nährstoffe nicht mehr wahrnehmen können.
Neben den oben genannten Medikamenten können auch einzelne andere Zytostatika (wie Cyclophosphamid, Methotrexat, Melphalan, Lomustin und Temozolomid) zu Nierenfunktionsstörungen führen. Das gilt vor allem dann, wenn sie in hoher Dosierung verabreicht werden, beispielsweise im Rahmen einer Hochdosis-Chemotherapie und/oder bei der Behandlung eines Krankheitsrückfalls.
Strahlentherapie
Auch eine Bestrahlung im Bereich der Nieren kann in manchen Fällen zu einer Nierenschädigung führen. Dies gilt vor allem dann, wenn größere Nierenareale bestrahlt werden müssen und eine Strahlendosis von 20 Gray (Gy) und mehr notwendig sind.
Krankheitsbilder
Die Funktion der Nieren kann durch die Therapie auf verschiedene Weise beeinträchtigt sein und so zu unterschiedlichen Krankheitsbildern führen. Ort und Ausmaß der Schädigung spielen dabei eine wesentliche Rolle.
Eine Schädigung der Nierenkörperchen (zum Beispiel durch Platinderivate) kann zur Folge haben, dass die Filter für größere Eiweiße (Proteine) oder auch rote Blutkörperchen durchlässiger werden, so dass diese nun ungehindert passieren können und dem Körper dadurch verloren gehen. Im Urin befindet sich dann zu viel Eiweiß (so genannte Proteinurie) oder Blut (Hämaturie). Andererseits kann es sein, dass zu viel Wasser zurückgehalten und in das Gewebe eingelagert wird. Es kommt dann zur Bildung von Ödemen.
Wenn die Nierenkanälchen (Tubuli) geschädigt sind (zum Beispiel durch Ifosfamid), kann die Rückgewinnung von lebenswichtigen Mineralstoffen sowie von Zucker und Aminosäuren aus dem Primärharn ins Blut beeinträchtigt sein. Diese Stoffe werden dann mit dem Urin ausgeschieden und stehen für ihre vielfältigen Aufgaben im Körper nicht mehr in ausreichend Menge zur Verfügung. Darüber hinaus kann die Ausscheidung von Stoffwechselendprodukten (wie Harnsäure) und Medikamenten (zum Beispiel Antibiotika) gestört sein, so dass diese sich als Gifte im Körpergewebe ansammeln und ablagern.
Unabhängig davon, welche Funktionsstörungen im Einzelnen vorliegen: Die Zerstörung von Nierengewebe und der damit einhergehende Leistungsverlust der Nieren (Niereninsuffizienz) kann letztlich zum Nierenversagen führen. Die Ärzte unterscheiden zwischen akutem und chronischem Nierenversagen. Während das akute Nierenversagen plötzlich auftritt, entwickelt sich ein chronisches Nierenversagen über Monate und Jahre hinweg. Beide Formen sind lebensbedrohlich für den Patienten und müssen daher behandelt werden.
Eine schwere Nierenschädigung kann außerdem Bluthochdruck, Vitamin-D-Mangel und Blutarmut (Anämie) verursachen und infolgedessen mit weiteren Organschäden verbunden sein.
Symptome einer Nierenschädigung
Nierenerkrankungen bereiten oft über lange Zeit keine Beschwerden. Mit zunehmendem Funktionsausfall der Nieren können sich folgende Symptome zeigen.
- Veränderungen beim Wasserlassen: Bei einer Nierenschwäche können sich die Menge und/oder die Konsistenz (das Aussehen) des Urins verändern: Die Harnausscheidung kann abnehmen oder ganz aufhören. Der wenige, noch ausgeschiedene Urin ist dann sehr hell, weil die Nieren den Harn nicht mehr konzentrieren können. Wenn der Urin schaumig aussieht, kann dies auf zu viel Eiweiß im Urin (Proteinurie) hinweisen. Eine rote oder rotbraune Färbung des Urins kann bedeuten, dass sich Blut im Urin befindet (Hämaturie).
- Flüssigkeitsansammlungen im Körper: Die Nieren regulieren die Menge der Flüssigkeit im Körper. Eine Störung der Nierenfunktion kann dazu führen, dass überschüssiges Wasser nicht mehr ausgeschieden wird (siehe oben), sondern sich im Gewebe ablagert. Dadurch kommt es an unterschiedlichen Körperstellen zu Schwellungen (Ödemen), zum Beispiel im Bereich der Fußgelenke, Füße, Unterschenkel, Hände und Augenlider sowie im Gesicht. Eventuell tritt auch Atemnot durch Wassereinlagerungen in der Lunge (Lungenödem) auf.
- Hoher Blutdruck: Die kranke Niere kann ihre Rolle bei der Regulation des Blutdrucks nicht mehr wahrnehmen, so dass sich mit fortschreitender Erkrankung ein Bluthochdruck entwickelt. Herz-Rhythmus-Störungen können die Folge eines gestörten Mineralstoffhaushalts (mit Anstieg des Kaliumsspiegels im Blut) sein.
- Allgemeine Erschöpfung, Abgeschlagenheit, Müdigkeit: In gesundem Zustand produzieren die Nieren das Hormon Erythropoetin (EPO), das die Bildung der roten Blutkörperchen anregt. Diese wiederum versorgen den Körper (vor allem Gehirn und Muskeln) mit Sauerstoff. Ein Nierenschaden kann dazu führen, dass weniger oder gar kein EPO mehr gebildet wird. Dies führt rasch zu einer Blutarmut (Anämie) und dadurch zu Müdigkeit und Erschöpfung. Ähnliche Symptome entstehen, wenn sich Abbauprodukte und Gifte, die normalerweise mit dem Urin ausgeschieden werden, im Körper ansammeln.
- Appetitlosigkeit, Übelkeit: (zum Teil mit Erbrechen und Durchfall), können infolge unbeseitigter Abfallstoffe im Körper hervorgerufen werden.
- Juckreiz, Veränderung der Hautfarbe, Blutergüsse: Ausschläge und Reizungen der Haut treten (durch die Verunreinigung des Blutes) ebenfalls häufig bei ungesunden Nieren auf. Da die hohe Giftkonzentration im Blut zu einer Funktionsstörung der Blutplättchen führt, kommt es leicht zu Blutergüssen.
- Schlechtes Wachstum im Kindesalter: Ein Funktionsverlust der Niere kann mit einer Störung des Calciumhaushaltes einhergehen, die einen Knochenum- und -abbau bewirkt. Das Knochenwachstum eines Kindes ist dadurch in besonderem Maße beeinträchtigt.
Wenn Sie eines oder mehrere der oben genannten Symptome an Ihrem Kind feststellen, sollten Sie auf jeden Fall einen Arzt konsultieren, um die Ursache zu klären. Je früher eine Nierenschädigung erkannt wird, umso besser lässt sie sich behandeln beziehungsweise aufhalten.
Risikofaktoren auf einen Blick
Wie hoch das Risiko einer Nierenschädigung als Folge der Krebstherapie ist, hängt von verschiedenen Faktoren ab. Ein erhöhtes Risiko besteht zum Beispiel:
- bei einer Chemotherapie mit folgenden Zytostatika: Cisplatin, Carboplatin, Ifosfamid, Cyclophosphamid, Methotrexat, Melphalan, Lomustin (CCNU) und Temozolomid
- bei einer hohen Dosierung dieser Zytostatika
- bei einer Strahlentherapie im Bereich der Nieren (ab 20 Gy)
- bei Patienten, die bei der Tumorbehandlung unter fünf Jahre alt sind
- wenn bereits vor der Therapie Nierenfunktionsstörungen bestanden haben
- innerhalb der ersten drei Jahren nach Therapieende
Bei welchen Krebskrankheiten kann es therapiebedingt zu Spätfolgen an den Nieren kommen?
Patienten, die im Rahmen ihrer Krebsbehandlung eine Chemotherapie mit den genannten Medikamenten und/oder eine Strahlentherapie im Bereich der Nieren erhalten, müssen auf lange Sicht unter Umständen mit einer Nierenschädigung rechnen. Die genannten Therapien werden derzeit vor allem bei folgenden Krebserkrankungen angewandt:
- akute lymphoblastische Leukämie (Ifosfamid, Cyclophosphamid, Methotrexat; bei SZT auch Melphalan)
- akute myeloische Leukämie (Cyclophosphamid bei SZT)
- Hodgkin-Lymphom (Cyclophosphamid; Melphalan und Ifosfamid bei SZT; unter Umständen Bestrahlungen im Nierenbereich)
- Non-Hodgkin-Lymphom (Ifosfamid, Cyclophosphamid, Methotrexat; Melphalan bei autologer SZT)
- niedrigmaligne Gliome (Platinderivate wie Cisplatin und Carboplatin; Cyclophosphamid )
- hochmaligne Gliome (Cisplatin, Carboplatin, Ifosfamid, Lomustin, Methotrexat, Temezolomid)
- Medulloblastom / ZNS-PNET (Cisplatin, Carboplatin, Methotrexat, Cyclophosphamid, Lomustin)
- Ependymom (Cisplatin, Carboplatin, Methotrexat)
- Osteosarkom (Cisplatin, Carboplatin, Methotrexat, Ifosfamid; Strahlentherapie spielt keine nennenswerte Rolle, da i.d.R. nur palliativ)
- Ewing-Sarkom (Ifosfamid, Cisplatin, Cyclophosphamid; bei Hochdosistherapie mit Melphalan; unter Umständen Strahlentherapie)
- Weichteilsarkome und Weichteiltumoren (Ifosfamid, Carboplatin – je nach Risikogruppe und Tumorart; unter Umständen Strahlentherapie im Bereich der Nieren)
- Neuroblastom (Carboplatin, Cisplatin, Ifosfamid, Cyclophosphamid, unter Umständen Strahlentherapie)
- Wilms-Tumor (Carboplatin und Cyclophosphamid bei besonders bösartigen Tumoren und fortgeschrittenen Krankheitsstadien; Strahlentherapie)
- Keimzelltumoren (Cisplatin, Ifosfamid)
- Hepatoblastom (Cisplatin, Carboplatin, Ifosfamid)
- Retinoblastom (Carboplatin)
Wichtig zu wissen: Jeder Patient wird individuell behandelt. Das heißt, selbst wenn Sie oder Ihr Kind an einer der oben genannten Krankheiten leiden, muss das nicht bedeuten, dass in jedem Fall eines der erwähnten Medikamente eingesetzt wird oder eine Bestrahlung der Niere erfolgt. Denn die Art der Therapie richtet sich stets auch nach Typ, Stadium und Verlauf einer Erkrankung und/oder der Lage eines Tumors. Auch führt nicht jede derartige Behandlung notgedrungen zu Spätfolgen. Die Höhe der Medikamenten- und Strahlendosis spielt dabei eine entscheidende Rolle. Ebenso kann die persönliche Konstitution und Veranlagung des Patienten von Bedeutung sein.
Fragen Sie Ihr Behandlungsteam, ob bei Ihnen beziehungsweise Ihrem Kind durch die Therapie ein erhöhtes Risiko für eine Nierenschädigung besteht!
Nachsorgeempfehlungen
Damit eine eventuelle Nierenschädigung rechtzeitig erkannt wird, empfehlen die Experten eine regelmäßige Kontrolle der Nierenfunktion. Dazu sollte in den ersten drei Jahren nach Ende der Behandlung mindestens einmal jährlich eine Blut- und Urinuntersuchung erfolgen.
Die Termine für die jährlichen Kontrolluntersuchungen sollten unbedingt eingehalten werden, auch dann, wenn es keine körperlichen Anzeichen einer Nierenschädigung gibt. Veränderungen der Niere können oft lange unbemerkt bleiben. Denn die enorm große Zahl an Nephronen kann Schädigungen über einen langen Zeitraum hinweg „vertuschen“.
Sind die Untersuchungsergebnisse nach Ablauf der ersten drei Jahren unauffällig, kann auf weitere Kontrollen verzichtet werden.
Achten Sie auf die Einhaltung der empfohlenen Kontrolltermine in den ersten drei Jahren:
1 x jährlich Blut und Urin untersuchen lassen!
Literatur 
- Stöhr W, Paulides M, Bielack S, Jürgens H, Koscielniak E, Rossi R, Langer T, Beck JD: Nephrotoxicity of cisplatin and carboplatin in sarcoma patients: a report from the late effects surveillance system. Pediatric blood & cancer 2007, 48: 140 [PMID: 16724313]
- Stöhr W, Paulides M, Bielack S, Jürgens H, Treuner J, Rossi R, Langer T, Beck JD: Ifosfamide-induced nephrotoxicity in 593 sarcoma patients: a report from the Late Effects Surveillance System. Pediatric blood & cancer 2007, 48: 447 [PMID: 16628552]